- 항체 기반 거래 41.2%…전임상 단계도 고밸류 계약 급증
- 비만·대사·희귀질환 23.5%…다중 조절·유전자 편집 기술 포함
- AI·RNA·유전체 플랫폼 29.4%…단일 후보보다 ‘생성 능력’ 확보로 이동
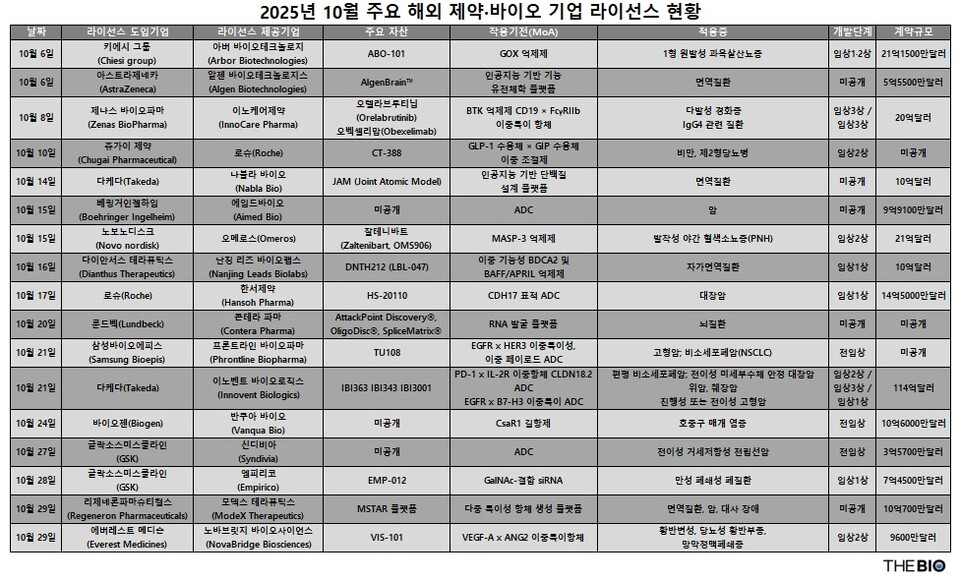
[더바이오 성재준 기자] 지난 10월 한 달 동안 글로벌 제약바이오 기업 간 총 17건의 기술이전(라이선스) 및 파트너십 거래가 체결된 것으로 나타났다. 항체약물접합체(ADC)와 이중항체를 포함한 항체 엔지니어링 기반 협업이 주요 흐름이었으며, 비만·대사·희귀질환 분야와 인공지능(AI)·리보핵산(RNA)·유전체 기반 플랫폼 확보를 위한 거래도 함께 이뤄졌다. 단일 품목 중심에서 다중 파이프라인을 고려한 거래가 늘어나는 움직임도 확인되고 있다.
최근 국가신약개발사업단(KDDF)이 공개한 ‘2025년 10월 신약 개발 관련 주요 딜(Deal)’ 자료에 따르면, 지난달 공개된 라이선스 거래 규모는 총 258억7600만달러(약 38조2200억원)로 집계됐다. 이 중 ADC·이중항체 관련 거래는 162억9400만달러(약 24조원)로 전체의 63%, 비만·대사·희귀질환은 52억2200만달러(약 7조7100억원)로 20.2%, AI·RNA·유전체 플랫폼은 33억700만달러(약 4조8800억원)로 12.8%를 차지한 것으로 나타났다. 나아가 전임상~초기 임상 단계 자산임에도 높은 가치로 계약된 사례가 나타나며, 장기 성장성과 기술 전환 가능성을 중시하는 움직임도 보이고 있다.
◇항체 기반 모달리티가 시장 주도…멀티스페시픽과 ADC 쏠림 심화
10월 거래에서 가장 두드러진 흐름은 항체 기반 기술의 비중 확대다. 전체 거래의 41.2%가 항체 기반 자산이었고, 규모 기준으로는 63%를 차지했다. 주요 사례로는 다국적 제약사 로슈(Roche)와 중국 한소파마(Hansoh Pharma)의 CDH17 표적 ADC 후보물질인 ‘HS-20110(개발코드명)’, 베링거인겔하임(Boehringer Ingelheim)과 국내 바이오기업 에임드바이오(Aimed Bio)의 ADC 기반 기술, 삼성바이오에피스(Samsung Bioepis)와 미국 프론트라인바이오파마(Phrontline Biopharma)의 EGFR×HER3 이중표적 듀얼페이로드 ADC 기반 기술을 적용한 ‘TH108(개발코드명)’, 다케다(Takeda)와 중국 이노벤트바이오로직스(Innovent Biologics, 이하 이노벤트)의 PD-1×IL-2R·CLDN18.2·B7-H3 기반 패키지 딜 등이 포함됐다.
전임상 또는 초기 임상 단계 자산에도 높은 계약 가치가 형성된 점도 특징이다. 114억달러(약 16조8300억원) 규모의 다케다와 중국 이노벤트 계약, 14억5000만달러(약 2조1400억원) 규모의 로슈와 한소파마 계약, 9억9100만달러(약 1조4600억원) 규모의 베링거인겔하임과 에임드바이오 계약 등 고액 거래가 이어졌으며, 이들 계약은 10월 초에만 4건 연속으로 체결돼 시장 초기부터 수요가 집중됐다.
이같은 흐름은 항체 기반 모달리티가 단일 후보물질을 확보하는데 그치기보다는 플랫폼 확장성이나 다적응증 적용 가능성, 파이프라인 보완 효과 등을 고려한 형태의 거래가 병행되고 있음을 보여준다. 초기 단계임에도 높은 밸류에이션이 적용된 사례가 확인되며, 개발 위험 외에도 선점과 조기 확보 요소가 거래 판단에 반영되고 있는 것으로 관찰된다.
국내 기업 참여도 확인됐다. 에임드바이오는 다국적 제약사와 ADC 공동 개발 협력을 진행한 사례이며, 삼성바이오에피스는 글로벌 기업들과 동일하게 라이선스를 도입한 형태로 분류된다.
고형암을 비롯해 미세부수체 안정형(MSS) 대장암, 췌장암, 전이성 종양 등에서 항체 기반 기술의 적용 범위가 확장되는 사례도 나타났다. 항체 기반 기술은 혈액암뿐만 아니라 고형암 영역으로 개발이 이어지고 있으며, 기존에 치료 선택지가 제한적이었던 환자군에서도 적용 가능성이 검토되는 상황이다.
미국 리제네론파마슈티컬스(Regeneron Pharmaceuticals)와 미국 모덱스테라퓨틱스(ModeX Therapeutics)의 ‘멀티스페시픽’ 항체 생성 플랫폼 사례처럼 단일 품목 확보를 넘어 ‘제품군 생성 능력’을 선제적으로 확보하려는 움직임도 관찰됐다. 이러한 플랫폼 중심 전략은 후보물질 전개 속도, 모듈형 개발 구조, 적응증 확장 유연성 측면에서 경쟁력을 제공해 기술 거래 평가 기준이 변화하고 있음을 보여준다.
◇비만·대사·희귀질환으로 확장…종양 중심 구조에서 이동 조짐
비만·대사·희귀질환 관련 거래는 4건(23.5%)이며, 규모 기준으로는 20.2%로 집계됐다. 비만 영역에서는 글루카곤 유사 펩타이드1(GLP-1) 단일 기전보다 포도당 의존성 인슐린 분비 촉진 폴리펩타이드(GIP)·글루카곤(GCG) 경로를 함께 고려한 다중 조절 접근법이 확인됐다. 희귀질환에서는 간 전달 기반 유전자 편집 기술이 포함됐다. 해당 거래는 대부분 전임상 또는 초기 임상 단계 자산으로 구성됐으며, 권리 구조는 지역별 독점 방식이 주로 적용됐다.
해당 사례에는 일본 쥬가이(Chugai)가 로슈에서 ‘GLP-1 수용체’와 ‘GIP 수용체’를 동시에 조절하는 듀얼 모듈레이터인 ‘CT-388(개발코드명)’을 도입한 것도 포함된다. 덴마크 노보노디스크(Novo Nordisk)와 미국 오메로스(Omeros)의 MASP-3 억제제, 이탈리아 키에지(Chiesi)와 미국 아버바이오테크놀로지스(Arbor Biotechnologies)의 원발성 과옥살산뇨증 유전자 편집 계열 자산도 여기에 해당된다. 또 영국 글락소스미스클라인(GSK)과 미국 알젠바이오테크놀로지스(Algen Biotechnologies)의 AI 기반 기능유전체학 플랫폼 ‘알젠브레인(AlgenBrain)’도 포함됐다. 다만 쥬가이는 로슈그룹 내 자회사라는 점에서 외부 기술이전과는 성격이 다소 다르다.
◇플랫폼 선점 우선 전략…AI·RNA·유전체 기반 거래 29.4%
AI·RNA·유전체 기반 플랫폼 관련 거래는 5건(29.4%)이며, 규모 기준으로는 12.8%로 나타났다. 해당 사례에는 영국 아스트라제네카(AZ)와 미국 알젠바이오테크놀로지스(Algen Biotechnologies)의 AI 기반 기능유전체학 플랫폼, 일본 다케다(Takeda)와 미국 나블라바이오(Nabla Bio)의 AI 단백질 설계 기술이 포함됐다.
또 덴마크 룬드벡(Lundbeck)과 부광약품 자회사인 덴마크 콘테라파마(Contera Pharma)의 중추신경계(CNS) RNA 플랫폼, GSK와 미국 엠피리코(Empirico)의 GalNAc-siRNA 플랫폼, 미국 바이오젠(Biogen)과 캐나다 제네반트바이오사이언스(Genevant Biosciences)의 지질나노입자(LNP) 기반의 RNA 전달 기술도 여기에 해당된다.
이들 거래는 하나의 후보물질을 확보하는 방식이 아니라, 여러 후보물질을 만들어낼 수 있는 기술을 도입하는 형태가 중심을 이뤘다. 이를 통해 신약 탐색 기간을 줄이고, 파이프라인을 더 넓힐 수 있는 여지를 확보하려는 목적이 반영됐다. 개발 단계는 대부분 전임상 수준이었고, 권리 범위는 지역이나 적응증을 한정하는 조건이 주로 적용됐다. 특히 작은 간섭 RNA(siRNA), RNA 전달, AI 설계, 기능유전체 플랫폼 등이 포함되면서 모달리티를 넓히는 동시에 필요한 기술 구성 요소를 보완하려는 요구가 나타난 것으로 풀이된다.

